BBC News Mundo
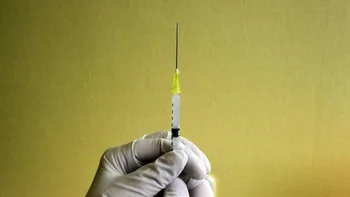
"Derecho a probar": la nueva ley firmada por Trump que legaliza tratamientos experimentales para enfermos terminales
nullSalvaremos miles y miles de vidasnull.

Así lo aseguró este miércoles el presidente estadounidense Donald Trump tras firmar la ley conocida como nullderecho a probarnull, que legaliza los tratamientos experimentales para pacientes con enfermedades terminales para las que la medicina común aún no encontró remedio.
Hasta ahora, los pacientes podían solicitar a la Administración de Alimentos y Medicamentos de Estados Unidos (FDA, por sus siglas en inglés) el acceso a medicamentos sin aprobación y la mayoría recibía el permiso.
Con la nueva norma, la FDA no tendrá derecho a supervisar los tratamientos experimentales como hasta ahora y únicamente será informada una vez programados.
Las farmacéuticas, por su parte, serán las que decidan dar luz verde o no a estos tratamientos y no estarán obligadas a dar acceso a medicamentos no aprobados para los pacientes que lo soliciten.
Por este motivo, la medida causa polémica y rechazo por parte de grupos de defensa de pacientes terminales que sostienen que esta ley no tendrá gran impacto en el aumento del acceso a ese tipo de tratamientos.
No obstante, la Cámara de Representantes aprobó la legislación la semana pasada después de que el Senado también diera el visto bueno en agosto, pasos previos a que Trump convirtiera este miércoles la propuesta legislativa en ley.

¿Qué cambia con esta ley?
La ley nullderecho a probarnull permite a los pacientes con enfermedades potencialmente mortales eludir el proceso de solicitud a la FDA para el nulluso compasivonull de medicamentos experimentales.
Los pacientes que buscan acceso a nullmedicamentos en investigaciónnull ahora solo necesitan la aprobación de su médico y del fabricante del mismo.
Para acceder a esta opción, los pacientes deben haber agotado todos los demás tratamientos aprobados y opciones de ensayos clínicos.
La nueva ley protege a los médicos y las empresas de los riesgos legales de permitir tratamientos no aprobados, a menos que dañen nullintencionalmentenull a un paciente.
¿Por qué hay preocupación?
El comisionado de la FDA, Scott Gottlieb, médico y sobreviviente de cáncer, expresó su preocupación al Congreso de EE.UU. el año pasado, incluso cuando dijo que la agencia estaba lista para implementar el proyecto de ley.
nullEl proceso de prueba clínica es crucial para el desarrollo de nuevos productos médicos innovadores que pueden mejorar o salvar la vida de los pacientesnull, dijo.
Gottlieb advirtió que tenía que haber un equilibrio entre dar a los pacientes acceso a terapias de investigación y pruebas que aseguren que los nuevos productos sean seguros y efectivos.

Bajo las reglas previas de la FDA sobre el nulluso compasivonull de este tipo de medicamentos, se aceptaron el 99% de las solicitudes de pacientes desde 2009.
La mayoría de los pedidos se aprobaron en el plazo de unos días, y en situaciones de emergencia, de manera inmediata por teléfono.
En particular, pasar por la FDA le permite a la agencia modificar los tratamientos experimentales para mejorar la seguridad del paciente.
Los grupos de defensa que se opusieron al proyecto afirmaron que la nueva ley da a los pacientes una falsa esperanza, ya que las compañías farmacéuticas no están obligadas a conceder a las personas con enfermedades terminales los tratamientos experimentales que soliciten.
En una carta dirigida al líder del Partido Republicano en el Congreso Paul Ryan y su par demócrata Nancy Pelosi, 38 grupos dijeron que eliminar a la FDA del proceso nullprobablemente haría más daño que un biennull.
40 estados ya aprobaron sus propias leyes sobre nullderecho a probarnull.
¿Cómo aprueba medicamentos la FDA?

Los medicamentos deben pasar por varias fases de ensayos clínicos para ser aprobados por la FDA. Y puede demorar años.
Primero, la farmacéutica debe demostrar que la medicina es segura para los humanos.
Estos ensayos pueden tener hasta 30 pacientes. El 70% de los medicamentos pasan a la siguiente prueba.
Luego, el fabricante debe probar que el producto es un tratamiento efectivo para la condición para la que se comercializa. Es importante destacar que el medicamento no puede tener efectos secundarios graves.
Solo el 33% de ellos pasa esta etapa.
Durante la siguiente fase, que puede llevar hasta cuatro años, la compañía debe evaluar el medicamento en entre 300 y 3.000 pacientes que padezcan la enfermedad para la que está diseñado.
Ahora puedes recibir notificaciones de BBC News Mundo. Descarga la nueva versión de nuestra app y actívalas para no perderte nuestro mejor contenido.