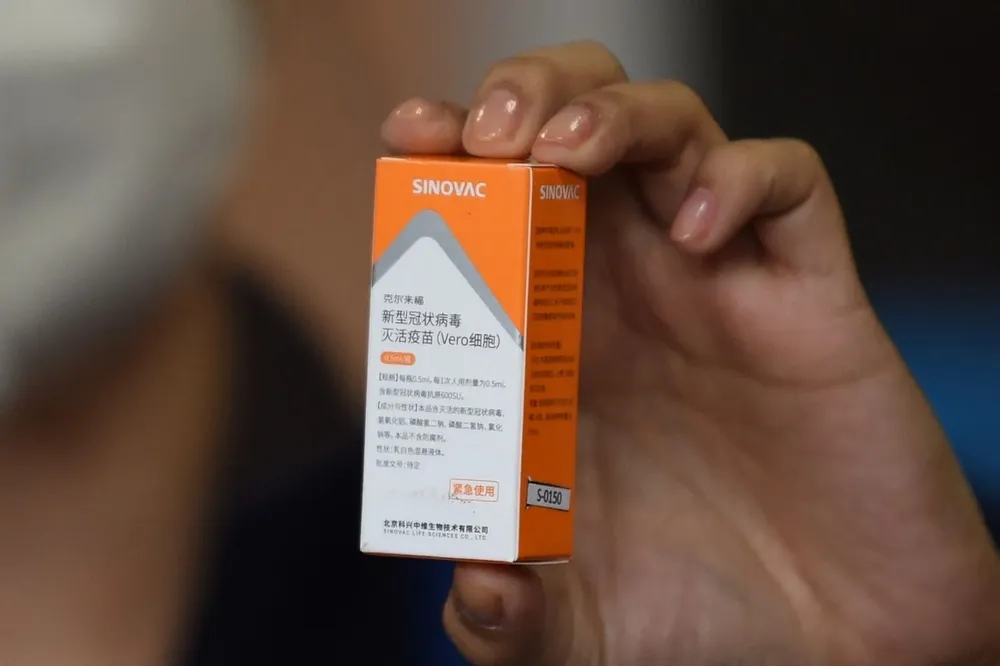
La Organización Mundial de la Salud (OMS) aprobó este martes el uso de emergencia de la vacuna china anticovid Sinovac, la más utilizada en Uruguay para combatir al coronavirus, informó la organización en un comunicado.
El comité de expertos en vacunas de la OMS recomendó la vacuna, que requiere dos dosis a intervalos de entre dos y cuatro semanas para personas de 18 años o más. En Uruguay se administra a personas de entre 18 y 70 años, y hasta este martes se aplicaron 2,1 millones de dosis, (75% del total de las vacunas anticovid aplicadas en el país).
Se trata del segundo inmunizante chino aprobado por la OMS, y a partir de ahora también podrá ser utilizado para el mecanismo Covax de distribución de vacunas anticovid, sobre todo en países desfavorecidos. El 7 de mayo, la OMS había aprobado la vacuna Sinopharm, fabricada en Pekín.
"El mundo necesita desesperadamente numerosas vacunas anticovid-19 para hacer frente a las enormes desigualdades en todo el planeta", declaró Mariangela Simao, subdirectora general de la OMS, encargada del acceso a los medicamentos y a los productos sanitarios. La efectividad de la Coronavac –el nombre del inmunizante de Sinovac– para prevenir los casos de covid-19 sintomáticos es de 57%, del 95% para prevenir el ingreso a CTI y del 97% sobre la muerte después de 14 días de recibida la segunda dosis, de acuerdo a un estudio preliminar realizado en Uruguay divulgado el jueves.
Estudios más avanzados en Chile mostraron que la vacuna presenta 65,3% de efectividad en la prevención del covid-19 sintomático, 90,3% en la prevención de ingreso en CTI y 86% en la mortalidad, aunque en ese país se vacunó a mayores de 70 años con esta fórmula, algo que no ocurrió en Uruguay.
Este suero, del tipo de virus inactivado, "es fácil de almacenar, lo que hace que sea fácil de gestionar y que esté especialmente adaptado a los países con pocos recursos", subrayó la agencia de la ONU.
La organización también ha aprobado el uso de las vacunas de Moderna, de Pfizer-BioNTech, las dos de AstraZeneca fabricadas en India y en Corea del Sur (aunque el producto sea idéntico, la OMS las contabiliza como dos vacunas distintas a la hora de dar su aprobación) y la de Johnson & Johnson, llamada "Janssen".
Este procedimiento ayuda a aquellos a países que no tienen medios para determinar por sí mismos la eficacia y la inocuidad de un medicamento, a poder acceder más rápidamente a las medicinas. Además, permitirá que el sistema Covax pueda contar con vacunas suplementarias. El sistema Covax fue puesto en marcha por la OMS con la Alianza Mundial para las Vacunas y la Inmunización (Gavi) y la Coalición para las Innovaciones en Preparación para Epidemias (CEPI) para distribuir vacunas contra el covid-19, especialmente en países pobres, pero ha tenido grandes atrasos en la entrega de las dosis.
Ingreso a Europa
La aprobación de la vacuna por parte de la OMS puede significar un cambio para el ingreso de personas vacunadas con las dosis de este laboratorio a territorio europeo. Hasta ahora, la Unión Europea (UE) solo permite el ingreso a extranjeros que tengan las vacunas autorizadas por la Agencia Europea de Medicamentos (EMA), que son la de Pfizer-BioNTech, Moderna, AstraZeneca y Johnson & Johnson. Algunos países, como España, aceptan además el ingreso de turistas que estén vacunados con inmunizantes aprobados por la OMS.
La Agencia Europea de Medicamentos (EMA) había decidido poner a revisión la vacuna china de Sinovac, la principal utilizada en Uruguay y aplicada en –al menos– 22 países. La aprobación de este martes por parte de la OMS deja vía libre para que, como ya sucedió con otros fármacos, la Unión Europea (UE) se encamine a validarla una vez que finalice el proceso.
Para que el proceso concluya con su aprobación, el órgano deberá seguir de cerca los resultados previos –que ya dio a conocer el laboratorio en sus ensayos clínicos– y determinar que cuenta con la información suficiente para garantizar su eficacia. Desde entonces, la empresa podrá sellar una solicitud formal para lanzarse al mercado y obtener su licencia de uso de emergencia, como la que ya tiene desde febrero en China, Chile, Brasil, Filipinas, Ucrania, Turquía y Uruguay, entre otros.
En caso de que Sinovac sea validada en Europa, los uruguayos que hayan recibido la inyección del laboratorio y cuenten con su certificado digital obtendrán facilidades en la circulación para, por ejemplo, ingresar a determinados sitios. De lo contrario, para viajar a Europa necesitarán presentar un test PCR con resultado negativo, como se les exige actualmente a los viajeros.
El ministro de Salud Pública, Daniel Salinas, aseguró en su cuenta de Twitter que la aprobación de Sinovac reafirma "la seriedad del trabajo realizado por la Comisión Nacional Asesora de Vacunas" así como la del grupo ad-hoc y de la división de Epidemiología de la cartera.
AFP